Содержание статьи
Название дано в честь А. Иерсена. К роду Yersinia относятся несколько видов, из которых для человека патогенны Y. pestis, Y. enterocolitica, Y. pseudotuberculosis. Они представляют собой грамотрицательные неспорообразующие палочки. Их различают по биохимическим, антигенным и другим признакам.
Иерсинии чумы
Возбудитель чумы Y. pestis был открыт А. Иерсеном в 1894 г.Морфология и физиология
Короткие с закругленными концами палочки, имеющие бочкообразную форму. Окрашиваются метиленовым синим биполярно. Спор не образуют, жгутиков не имеют. Образуют капсулу (рис. 20.16 на цв. вкладке, 20.17). Y. pestis являются гетеротрофными бактериями, нетребовательными к питательным средам. Растут в широком диапазоне температур (5°-37°С). На агаровых средах образует плоские с неровными краями колонии, напоминающие кружевной платочек. На жидких средах образуются хлопья и рыхлый осадок. Ферментирует с образованием кислоты ряд Сахаров (табл. 20.10.). Возбудитель чумы продуцирует гиалуронидазу, фибринолизин, коагулазу, протеинкиназу.Антигены
Y. pestis имеет несколько антигенов. Антиген F1 представляет собой основной компонент поверхностной структуры бактериальных клеток белковой природы. V-антиген также является белком, W-антиген - липопротеидным комплексом. Эти антигены связаны с клеточной стенкой. Y. pestis имеет перекрестные антигены с другими иерсиниями и энтеробактериями (Е. coli, Salmonella), а также с эритроцитами человека О-группы.Патогенностъ и патогенез
Вирулентность возбудителя чумы связана прежде всего с его адгезией на эпителиальных клетках разных органов и тканей в зависимости от входных ворот инфекции. В адгезии участвует капсула и поверхностные структуры клеточной стенки. В инвазии, агрессии (подавлении фагоцитарной активности макрофагов) участвуют различные ферменты и токсины, продуцируемые этими бактериями. Существенное значение в патогенности Y. pestis имеет «мышиный» токсин, который блокирует функции клеточных митохондрий печени и сердца, а также вызывает образование тромбов. «Мышиный» токсин относится к белковым токсинам, прочно связанным с бактериальной клеткой, синтез которого контролируется плазми-дой. Так же как и другие белковые токсины, он состоит из двух субъединиц, одна из которых ответственна за прикрепление токсина к клетке хозяина, другая - за токсические свойства. Наряду с ним токсичность и аллергизация организма связаны с ЛПС (эндотоксин) и другими компонентами клеточной стенки. Определенную роль в вирулентности чумных бактерий играют такие ферменты, как плазмокоагулаза и фибринолизин, локализованные в наружной мембране бактериальной клетки. При этом происходит нарушение активации комплемента и появление геморрагии и некрозов в лимфоузлах. Факторы патогенности закодированы в хромосоме и плазмидах.Патогенез и клинические формы
Патогенез и клинические формы чумы зависят от входных ворот инфекции. Различают кожную, бубонную, легочную и другие клинические формы чумы. При пониженной сопротивляемости организма большой дозе возбудителя может возникнуть первичная септическая форма болезни. Вторичный сепсис возникает при любой клинической форме чумы. При этом больные выделяют возбудителя с мочой, мокротой, калом. Первичная легочная форма чумы возникает при заражении аэрозольным путем, вторичная - гематогенно как осложнение. До появления антибиотиков смертность при чуме была очень высокой.Иммунитет
Постинфекционный иммунитет характеризуется высокой напряженностью, связанной с гуморальными (антителами) и клеточными (фагоцитоз) факторами.Экология и эпидемиология
Чума относится к зоонозным инфекциям с природной очаговостью. Резервуар инфекции - грызуны (суслики, тарабаганы, сурки, песчанки и др.). Переносчиками являются блохи. Вспышкам чумы среди людей обычно предшествуют эпизоотии среди грызунов. От человека к человеку чума передается воздушно-капельным путем только от больных легочной формой чумы.Чума
Чума - острая, зоонозная особенно опасна, карантинная инфекционная болезнь с поражениями кожи, лимфатических узлов, легких, геморрагической септицемией и интоксикацией. Возбудитель чумы - Yersiniapestis - принадлежит к роду Yersinia семейства Enterobacteriaceae. До этого рода входят еще два патогенных для человека виды иерсиний: Y. pseudotuberculosis, Y. enterocolitica. Кроме трех основных возбудителей иерсиниозив выделяют еще 8 видов, в инфекционной патологии человека значения не имеют, правда, некоторые из них могут изредка вызывать оппортунистические инфекции.Источником чумы в природе являются различные виды диких и домашних животных, грызунов, а переносчиками - их блохи. Проникая в человеческое сообщество, чумная инфекция может стать антропонозам, который распространяется в виде эпидемий и пандемий.Возбудитель чумы имеет несколько антигенов, из них наиболее изучены D-, F1-, Т-, V-, W. Но серологическое его типирование разработана еще недостаточно и в рутинной лабораторной практике не используется.Микробиологическое исследование проводится с целью диагностики заболевания, выявления инфицирования животных и переносчиков в эндемичных очагах и установления контаминации иерсинии различных объектов окружающей среды. При этом используют бактериоскопический, бактериологический, биологический и серологический методы, а также аллергическую пробу с пестином для ретроспективной диагностики. Первый случай заболевания чумой у человека должен быть обязательно подтвержден выделением возбудителя.Взятие материала
Взятие материала для исследования как все этапы выделения возбудителя и работы с грызунами или лабораторными животными проводят в противочумных костюмах первого типа. В лаборатории необходимо создать строгий противоэпидемический и дезинфекционный режимы, которые регламентированы специальными инструкциями. В зависимости от клинической формы чумы, от больного берут следующие материалы: выделения из язвы или карбункула (кожная форма); пунктат с бубона (бубонная форма), кровь (при всех формах), фекалии и спинномозговую жидкость (при поражениях кишечника или мозговых оболочек). Материал важно принять до начала антибиотикотерапии. При направлении секционного материала берут кровь, костный мозг, кусочки паренхиматозных органов. Кроме того, в лаборатории доставляют живых и погибших грызунов, блох, пищевые продукты, воду. В отдельных случаях исследуют воздух, смывы с поверхности объектов.Взятый материал помещают в стеклянные банки с притертыми пробками, обертывают вощаной бумагой, снаружи их обтирают 5% раствором лизола, наклеивают этикетку, на которой указывают дату, место, характер материала, фамилия больного, диагноз. Банки плотно укладывают в герметичную тару, надписывают "верх" и направляют служебным транспортом с доверенным лицом в ближайшей противочумной учреждения или лаборатории для диагностики особо опасных инфекций. Персонал, который проводил забор материала, подлежит полной санитарной обработке.Бактериоскопия
Из исследуемого материала в лаборатории изготавливают 5-6 мазков, фиксируют их этанолом или смесью спирта и эфира в течение 15-20 мин. Один мазок окрашивают по Граму, второй - метиленовой синькой, третий - меченой люминесцентной сывороткой против Y. pestis (прямая РИФ), 2-3 мазки оставляют в резерве. Обнаружение в мазках характерных, биполярно окрашенных, овоидные, грамотрицательных бактерий, которые дают к тому же специфическое люминесцентное свечение в виде яркого зеленоватого ореола вокруг клеток, при характерных клинических симптомах и учете эпидемиологической ситуации, дает право поставить предварительный диагноз чумы.Бактериологическое исследование
Несмотря на характерную клиническую картину заболевания, бактериологическое диагностику надо проводить обязательно во всех случаях. Для посевов используют высокопитательные среды с добавлением стимуляторов роста, хотя палочки чумы неприхотливы к питательным средам. Исследуемые материалы, не контаминированные посторонней микрофлорой (кровь, пунктат бормотал, ликвор), сеют во флаконы, содержащие 50-100 мл МПБ и параллельно в чашки с МПА или агаром Хотингера. Материал, загрязненный сопутствующей флорой, высевают на МПА с сульфитом натрия, среды Туманского (МПА с 1% гемолизированной крови и генциановый фиолетовым в концентрации 1:100000-1:400000) или коробочной (0,15% полужидкий агар с 0,3% гемолизированной крови и генциановый фиолетовым 1:200000). Для инактивации чумного фага на поверхность плотных сред наносят и равномерно распределяют 0,1 мл антифаговои сыворотки. Посевы выращивают при 28 ° С и 37 ° С.Через 18-20 ч в жидких средах появляется пленка со спущенными вниз нитевидными образованиями, подобными сталактитов, на дне образуется рыхлый осадок. Развитие колоний на плотных средах проходит три стадии. Через 10-12 ч под микроскопом рост напоминает скопление бесцветных пластинок (стадия "битого стекла"). Позднее (18-20 ч) образуются колонии с выпуклым мутно-белым центром, окруженным фестончатыми каймой (стадия "кружевной платочек"). Через 40-48 ч наступает фаза "взрослых колоний" с буроватым центром и зазубренные периферической зоной.С типичных колоний готовят мазки, окрашивают по Граму и метиленовым синим, производят пересев на скошенный агар (или бульон) для выделения чистой культуры. На следующий день, убедившись что культура чистая, приступают к ее идентификации. Для этого проводят реакцию агглютинации и преципитации с диагностическими антисыворотки против соматического и капсульного антигенов, ставят РНГА с лиофилизированными эритроцитарными антительным диагностику мамы, пробу на лизис чумным бактериофагом и заражают чистой культурой гвинейских свинок. Обязательно определяют антибиотикочувствительность дискодифузийним методом на агаре или методом серийных разведений в бульоне.Чистую культуру засевают в среды Гисса для определения ферментативных свойств. Возбудитель чумы разлагает до кислоты глюкозу, маннит, галактозу, левулезы, ксилозу, отдельные штаммы ферментируют арабинозу и глицерин.Свижовидилени штаммы не разлагаются адонит, рамнозу и сахарозу, не выделяют оксидазу, уреазу, но имеют фермент каталазу, не свертывают молоко, не образуют индол. Необходимо провести дифференциацию Y. pestis от других иерсиний.Визначальнмы признаками при идентификации возбудителя чумы является агглютинация культуры антисыворотки, лизис чумным бактериофагом и положительная биопроба.Биологическое исследования
Биологическое исследования при диагностике чумы обязательна. Биологическую пробу ставят как с первичным материалом, так и с выделенной чистой культурой. Для заражения используют гвинейских свинок, реже - белых мышей. Если материал не контаминированный сопутствующей микрофлорой (кровь, пунктат бубона), его вводят подкожно или внутрибрюшинно. При загрязнении материала посторонней флорой заражения проводят путем втирания эмульгированной материала в депильовану и скарификовану кожу живота гвинейской свинки. При положительной биопробе животные погибают через 2-3 дня при заражении в брюшную полость, или через 5-7 дней - при нанесении материала на кожу. Вскрывают погибших свинок, изучают патологоанатомические изменения: гиперемия сосудов, увеличение печени, селезенки, лимфатических узлов, наличие на их поверхности и на разрезе некротических участков. Из крови и паранхиматозних органов делают мазки и мазки-отпечатки, проводят посев на питательные среды. В мазках обнаруживают огромное количество биполярно окрашенных грамотрицательных овоидные палочек. Выделенные от животных чистые культуры идентифицируют так же, как и культуры после бактериологического исследования. Трупы гвинейских свинок, как исследуемых диких грызунов, погружают в 5% раствор лизола, а затем сжигают.Серологическая диагностика
Серологическая диагностика чумы не получила широкого применения. В последнее время проводят постановку РНГА с эритроцитарных диагностикумов, на котором адсорбированный капсульный антиген Y pestis. Диагностическим титром считают разведение сыворотки 1:40. Вообще же серологические реакции проводят обычно для ретроспективной диагностики и при массовых эпизоотических обследованиях грызунов в эндемичных очагах чумы.Ускоренные методы диагностики
Предложенные экспрессные методы выявления возбудителя чумы с помощью флуоресцентных антител, в РНГА с использованием антительных эритроцитарных диагностикумов. Они позволяют выявить Y. pestis в исследуемом материале через 2 часа.В ускоренных методов диагностики относят также реакцию преципитации в стандартных агаровых пластинках с противочумной сыворотки и метод быстрого роста возбудителя чумы на элективные среды с использованием бактериофага. Для этого 0,2-0,3 мл материала сеют в 4 пробирки со средой коробочной и 0,1 мл агар в чашке Петри. В одну из пробирок вносят 0,2-0,3 мл чумного фага. Посевы инкубируют при 28 ° С в течение трех часов. Из пробирок, в которых виден рост, готовят 2 мазки, окрашивают по Граму и метиленовым синим. При положительном результате в мазках видны цепочки грамотрицательных овоидные палочек, окрашенных биполярно. В пробирке с фагом роста нет. С пробирки с ростом по 0,4 мл материала вводят в брюшную полость нескольких мышей. Через 8-10 ч просматривают чашки с агаром для выявления роста возбудителя чумы.Через 10-12 ч забивают мышей, от них сеют экссудат и материал из паренхиматозных органов в пробирки с полужидким агаром и исследуют так же, как выше описано. Итак, предварительный результат получают через 4 часа, а окончательный - через 18-20 час.Для ретроспективной диагностики чумы используют аллергическую пробу с пестином.Профилактика и лечение
Специфическая профилактика проводится путем вакцинации живой или химической вакциной. Первая готовится из штамма EV. В РФ применяется живая вакцина. После однократного введения продолжительность иммунитета достигает 6 мес. Для лечения применяют стрептомицин и другие антибиотики.Чумна́я па́лочка (лат. Yersinia pestis ) - вид грамотрицательных бактерий из семейства энтеробактерий. Инфекционный агент бубонной чумы, также может вызывать чумную пневмонию и септическую чуму. Все три формы ответственны за высокий уровень смертности в эпидемиях, имевших место в истории человечества, например таких как «Юстинианова чума» (100 миллионов жертв) и «Чёрная смерть», на которой - смерть трети населения Европы за промежуток с 1347 по 1353 годы.
Роль Yersinia pestis в «Чёрной смерти» дискутируется. Некоторые утверждают, что «Чёрная смерть» распространилась слишком быстро, чтобы быть вызванной Yersinia pestis . ДНК этой бактерии найдены в зубах умерших от «Чёрной смерти», тогда как тестирование средневековых останков людей, умерших по другим причинам, не дало положительной реакции на Yersinia pestis . Это доказывает, что Yersinia pestis является как минимум сопутствующим фактором в некоторых (возможно, не во всех) европейских эпидемиях чумы. Возможно, что устроенный чумой отбор мог повлиять на патогенность бактерии, отсеяв индивидуумов, которые были наиболее ей подвержены.
Род Yersinia - грамотрицательные, биполярные коккобациллы. Так же, как и другие представители Enterobacteriaceae , они обладают ферментативным метаболизмом. Y. pestis производит антифагоцитарную слизь. Подвижная в культуре бактерия становится неподвижной, попав в организм млекопитающего.
История
Y. pestis была открыта в 1894 году швейцарско-французским медиком и бактериологом Пастеровского института Александром Йерсеном во время эпидемии чумы в Гонконге. Йерсен был сторонником школы Пастера. Прошедший подготовку в Германии японский бактериолог Китасато Сибасабуро, практиковавший метод Коха, также в это время был привлечён к поискам агента, являющегося возбудителем чумы. Однако именно Йерсен фактически связал чуму с Y. pestis . Долгое время возбудителя чумы относили к роду Bacterium , позже - к роду Pasteurella . В 1967 году род бактерий, к которому относился возбудитель чумы, был переименован в честь Александра Йерсена.
В результате сравнения древних штаммов генов Yersinia pestis и её вероятного предка Yersinia pseudotuberculosis (псевдотуберкулезная палочка) было выявлено, что Yersinia pestis мутировала из сравнительно безвредного микроорганизма около 10 тысяч лет назад. Выяснилось, что обитающая в почве Y. pseudotuberculosis , вызывающая легкое заболевание желудочно-кишечного тракта, приобрела тогда несколько генов, позволивших ей проникать в легкие человека. Далее, в ключевом гене Pla произошла замена одной аминокислоты, в результате чего микроорганизм смог с повышенной силой разлагать белковые молекулы в легких и размножаться по всему организму через лимфатическую систему. Исследователи подозревают, что ген Pla чумная палочка позаимствовала у другого микроба в результате горизонтального обмена генами. Это подтверждают и исследования датских и британских ученых, которые провели исследования молекул ДНК, извлеченных из зубов 101 человека бронзового века, обнаруженных на территории Евразии (от Польши до Сибири). Следы бактерии Y. pestis нашли в ДНК семерых, возрастом до 5783 лет, при этом в шести из этих образцов отсутствовали «ген вирулентности» ymt и мутации в «гене активации» pla. В дальнейшем, на рубеже второго и первого тысячелетия до нашей эры, из-за демографических условий, выразившихся в увеличении плотности населения, возникла более летальная «бубонная» мутация бактерии.
Известны три биовара бактерии; полагают, что каждый соответствует одной из исторических пандемий чумы. Биовар antiqua считают ответственным за Юстинианову чуму. Неизвестно, был ли этот биовар причиной более ранних, меньших эпидемий, или же эти случаи вообще не были эпидемиями чумы. Биовар medievalis полагают связанным с «Чёрной смертью». Биовар orientalis связывают с Третьей пандемией и большинством современных вспышек чумы.
Патогенность и иммунитет
Патогенность Yersinia pestis заключается в двух антифагоцитарных антигенах, называемых F1 и VW , оба существенны для вирулентности. Эти антигены производятся бактерией при температуре 37 °C. Кроме этого, Y. pestis выживает и производит F1 и VW антигены внутри кровяных клеток, таких, например, как моноциты, исключением являются полиморфно-ядерные нейтрофильные гранулоциты.
Некоторое время назад в США инактивированная формалином вакцина была доступна для взрослых, находящихся под большим риском заражения, однако затем продажи были прекращены по указанию FDA, специального агентства министерства здравоохранения США, по причине низкой эффективности и вероятности серьёзного воспаления. Ведутся перспективные эксперименты в генной инженерии по созданию вакцины, основанной на антигенах F1 и VW, хотя бактерии не имеющие антигена F1 сохраняют достаточную вирулентность, а антигены V достаточно изменчивы, так что вакцинация, основанная на этих антигенах может не давать достаточно полной защиты.
В России доступна живая вакцина на основе невирулентного штамма чумы.
Вакцинация не защищает от легочной чумы. Во время эпидемии 1910-1911 года применение прочумных сывороток (лимфы Хавкина и сыворотки Йерсена) лишь продлевало течение болезни на несколько дней, но не спасло жизнь ни одному больному. Впоследствии ученым окончательно стало ясно, что гуморальный иммунитет при аэрогенном инфицировании возбудителем чумы значения не имеет.
Геном
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis), штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США), штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 парных оснований, в штамме CO92 - 4 653 728 парных оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica , бактерия Y. pestis содержит плазмиды pCD1 . Вдобавок, она также содержит плазмиды pPCP1 и pMT1 , которых нет у других видов рода Yersinia . Перечисленные плазмиды и остров патогенности, названный HPI , кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов.
Лечение
С 1947 года традиционным средством первого этапа лечения от Y. pestis были стрептомицин, хлорамфеникол или тетрациклин. Также есть свидетельства положительного результата от использования доксициклина или гентамицина.
Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
Чумная палочка (лат. Yersinia pestis) - грамотрицательная бактерия из семейства энтеробактерий. Инфекционный агент бубонной чумы, также может вызывать пневмонию (легочную форму чумы) и септическую чуму. Все три формы ответственны за высокий уровень смертности в эпидемиях, имевших место в истории человечества, например таких как Великая чума и «Чёрная смерть», на счету последней из которых - смерть трети населения Европы за промежуток с 1347 по 1353 годы.
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis), штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США), штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 пар оснований, в штамме CO92 - 4 653 728 пар оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica, бактерия Y. pestis содержит плазмиды pCD1. Вдобавок, она также содержит плазмиды pPCP1 и pMT1, которых нет у других видов рода Yersinia. Перечисленные плазмиды и остров патогенности, названный HPI, кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов. Полагают, что бактерия Y. pestis произошла от Y. pseudotuberculosis, отличие только в присутствии специфичных вирулентных плазмид.
Традиционным средством первого этапа лечения от Y. pestis были стрептомицин, хлорамфеникол или тетрациклин. Также есть свидетельства положительного результата от использования доксициклина или гентамицина. Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
En:
Yersinia pestis is a Gram-negative rod-shaped bacterium belonging to the family Enterobacteriaceae.
It is a facultative anaerobe that can infect humansand other animals.Human Y. pestis infection takes
three main forms: pneumonic, septicemic, and the notorious
bubonic plagues. All three forms are widely believed to have been responsible for a number of
high-mortality epidemics throughout human history, including the Plague of Justinian in 542
and the Black Death that accounted for the death of at least one-third of the European
population between 1347 and 1353.
The complete genomic sequence is available for two of the three sub-species of Y. pestis: strain KIM (of biovar Medievalis), and strain CO92 (of biovar Orientalis, obtained from a clinical isolate in the United States). As of 2006, the genomic sequence of a strain of biovar Antiqua has been recently completed. Similar to the other pathogenic strains, there are signs of loss of function mutations. The chromosome of strain KIM is 4,600,755 base pairs long; the chromosome of strain CO92 is 4,653,728 base pairs long. Like its cousins Y. pseudotuberculosis and Y. enterocolitica, Y. pestis is host to the plasmid pCD1. In addition, it also hosts two other plasmids, pPCP1 (also called pPla or pPst) and pMT1 (also called pFra) which are not carried by the other Yersinia species. pFra codes for a phospholipase D that is important for the ability of Y. pestis to be transmitted by fleas. pPla codes for a protease, Pla, that activates plasminogen in human hosts and is a very important virulence factor for pneumonic plague. Together, these plasmids, and a pathogenicity island called HPI, encode several proteins which cause the pathogenesis, for which Y. pestis is famous. Among other things, these virulence factors are required for bacterial adhesion and injection of proteins into the host cell, invasion of bacteria in the host cell (via a Type III Secretion System), and acquisition and binding of iron that is harvested from red blood cells (via siderophores). Y. pestis is thought to be descendant from Y. pseudotuberculosis, differing only in the presence of specific virulence plasmids.
The traditional first line treatment for Y. pestis has been streptomycin, chloramphenicol,
tetracycline, and fluoroquinolones. There is also good evidence to support the use of doxycycline
or gentamicin. Resistant strains have been isolated; treatment should be guided by antibiotic
sensitivities where available. Antibiotic treatment alone is insufficient for some patients,
who may also require circulatory, ventilator, or renal support.
(Материал с
http://ru.wikipedia.org/wiki/Yersinia_pestis)
Yersinia pestis, the Gram-negative coccobacillus belonging to the Enterobacteriaceae is the causative
agent of plague and is arguably the deadliest pathogen in history. At least 200 million deaths have
been attributed to this disease in modern times.
Yersinia pestis was named after Andre Yersin the French bacteriologist sent by Institute Pasteur to
the Far East (Hong Kong) to study plague where he first isolated plague bacillus in 1894.
Yersinia pestis is primarily a rodent pathogen, with humans being an accidental host when bitten by
an infected rat flea. The flea draws viable Y. pestis organisms into its intestinal tract. These organisms
multiply in the flea and block the flea"s proventriculus (digestive chamber). Some Y. pestis in the flea
are then regurgitated when the flea gets its next blood meal thus transferring the infection to a new host.
Within hours of the initial flea bite, the infection spills out into the bloodstream, leading to involvement
of the liver, spleen, and lungs. The patient develops a severe bacterial pneumonia, exhaling large numbers
of viable organisms into the air during coughing fits. 50 to 60 percent of untreated patients will die if
untreated. As the epidemic of bubonic plague develops (especially under conditions of severe overcrowding,
malnutrition, and heavy flea infestation), it eventually shifts into a predominately pneumonic form, which
is far more difficult to control and which has 100 percent mortality.
The sequencing has revealed Y. pestis to be a highly dynamic and adaptable pathogen that has undergone rapid
genetic changes. It appears to have evolved in a remarkably short time from a relatively harmless stomach
bug to a blood-borne pathogen. Over time, Y. pestis acquired genes from other bacteria and viruses that
allowed it to live in the blood instead of the intestine, altogether, the researchers identified 21 regions,
or adaptation islands, that were probably acquired from other organisms.
Conversely, gene acquisition has been balanced by gene loss. 149 deactivated genes,
or pseudogenes, were discovered, that once enabled Y. pestis to thrive in the human
gut, but are no longer needed in the new environment. These include genes associated with adhesion,
mobility and colonization of the gut.
RUS:
Yersinia pestis, грамотрицательная коккобацилла из семейства Энтеробактерий, - возбудитель чумы и, возможно,
смертельнейший патоген в истории. По крайней мере 200 млн. смертей приписано этому заболеванию к настоящему
времени.
Yersinia pestis была названа в честь Андрэ Ерсина, французского бактериолога из Института Пастера на
Дальнем Востоке (Гонконг), где он впервые открыл чумную палочку в 1894 году.
Yersinia pestis - это преимущественно разъедающий патоген, человек стал ее случайным хозяином, когда
был укушен инфицированной крысиной блохой. Блоха несла жизнеспособных организмов Yersinia pestis в кишечном
тракте.Эти организмы размножились в блохе и закупорили ее провентрикулум (многокамерный пищеварительный канал).
Некоторые Yersinia pestis затем переносятся от блохи к новому носителю инфекции, когда у нее был следующий
кровавый обед.В течение часа после укуса блохи инфекция разносится по кровотоку, попадая в печень, селезенку и
легкие. У пациента развивается острая бактериальная пневмания, выдыхая огромное количество жизнеспособных
организмов во время кашля. От 5о до 60 % пациентов умирает, если не лечатся. Поскольку эпидемия бубонной чумы
развивается (особенно в условиях перенаселенности, недоедания и сильной инвазии блохами), это в конечном
счете переходит в преимущественную пневманическую форму, которую намного сложнее контролировать и которая
имеет стопроцентную смертность.
Последствия показали, что Yersinia pestis - чрезвычайно динамичный и приспосабливаемый патоген,
подверженный быстрым генетическим изменениям. С течением времени Yersinia pestis приобрелагены от других бактерий и вирусов,
которые позволили ей жить не в кишечнике, а в крови; всего исследователи идентифицировали 21 область, или
остров адаптации, которые мы, возможно, приобрели от других организмов.
Напротив, приобретение одних генов компенсируется утратой других. Было открыто 149 дезактивированных генов,
или псевдогенов, которые некогда позволяли Yersinia pestis процветать в человеческом кишечнике, но не
пригодившиеся больше в новом окружении. Эти включенные гены связаны с прилипанием, подвижностью и
колонизацией кишечника.
Запрос в БД PubMed: yersinia pestis complete genome 2000:2010
найдено: 30 статей
аннотация одной из статей: Sadovskaia NS, Mironov AA, Gel"fand MS.
Abstract
One of the main trends in the prokaryote genomics is the comparative analysis of metabolic pathways.
This method can be used for the analysis of experimentally studied systems of co-regulated genes,
as well as genes with unknown regulatory signals. In this study we apply the comparative analysis
of regulatory signals to the genes of the enzymes for fatty acid metabolism from Escherichia coli,
Haemophilus influenzae, Vibrio cholerae, Yersinia pestis. Transcription of these genes is regulated
by the FadR protein. We describe the FadR regulation of the long-chain fatty acid oxidation and partially
that of the fatty acid biosynthesis. We also demonstrate that the gene yafH encoding acyl-CoA dehydrogenase
is identical to the gene fadE, previously identified by genetic techniques.
EN:
Одна из главных черт генома прокариотического организма - это сравнительный анализ типов метаболизма.
Этот метод может быть использован для анализа экспериментальных данных о ко-регулируемых генах так же
хорошо, как для генов с неизвестными регуляторными функциями. В этом исследовании мы применяем
сравнительный анализ регуляторных сигналов к генам ферментов метаболизма жирных кислот у Escherichia coli,
Haemophilus influenzae, Vibrio cholerae, Yersinia pestis. Транскрипция этих генов регулируется FadR-белком.
Мы описываем FadR-регуляцию окисления длинных цепочек жирных кислот и частично то, что они синтезируют.
Мы также показываем, что ген yafH, кодирующий ацил-CoA дегидрогеназу идентичен гену FadR, идентифицированному
ранее с помощью генетической техники.
Чума относится к острым инфекционным заболеваниям. Она характеризуется лихорадкой, тяжелой интоксикацией, поражением лимфоузлов, кожи, легких. Отличительная особенность чумы в том, что она может быстро давать септическое течение. Эта болезнь признана одной из наиболее опасных инфекций.
Причины. Возбудитель
Как происходит заражение
Переносят чумную палочку в основном грызуны и зайцы – крысы, мыши, суслики. Те хищники, которые уничтожают грызунов, также могут стать переносчиками инфекции. В истории известно несколько крупных эпидемий этой болезни. Они связаны с миграцией крыс, которые заражаются в естественных очагах. Переносчиком инфекции с крысы на человека является блоха. При укусе человека блоха срыгивает в место укуса содержимое своего желудка, в котором находятся чумные палочки. Чумой могут заразиться и те люди, которые имеют дело с выделкой шкур, те, которые употребили в пищу зараженное мясо. Еще один путь для человека – воздушно-капельный (этим путем люди заражаются легочной формой чумы). Также чуму могут переносить клещи и вши. Стоит отметить, что человек очень восприимчив к чуме – после того, как человек переболел чумой, у него не формируется стойкого иммунитета, и он может заболеть еще раз.
Эпидемиология
Сейчас в мире есть районы, в которых зарегистрирована чума.
Эпидемии чумы имеют свои стадии:
- 1 стадия – чумная палочка находится у грызунов;
- 2 стадия – чумная палочка регистрируется и у грызунов, и у людей. На этой стадии у некоторых больных поражаются легкие, что провоцирует легочную форму чумы;
- 3 стадия – на этой стадии становится возможным передача чумы воздушно-капельным путем.
Клиника
Если человеку попадает в организм чумная палочка, то на месте проникновения (укуса) возникает ответная реакция организма – пустула с кровью или маленькая язвочка. Затем по лимфатическим сосудам возбудитель перемещается в лимфатические узлы. Здесь на чумную палочку пытаются воздействовать мононуклеарные клетки-фагоциты. Однако их действие подавляется возбудителем. Они не только не уничтожаются, но и размножаются внутриклеточно, провоцируя воспалительную реакцию. Она продолжается в организме приблизительно неделю. Из-за того, что чумная палочка размножается, лимфатические узлы резко увеличиваются, сливаются и образуют укрупнения – бубоны. На этом этапе палочка устойчива к фагоцитозу. При этом в лимфоузлах происходит геморрагический некроз, микроорганизмы в результате имеют возможность внедриться в кровеносные сосуды. После этого они разносятся по всему организму. Септическая форма сопровождается характеризуется поражением почти всех органов и формированием новых бубонов. Наиболее опасны заносы инфекции в легкие – отсюда болезнь переносится воздушно-капельным путем. По статистике эта форма занимает около двадцати процентов. При проникновении в легкие развивается геморрагический некроз с образованием выпота. Одновременно развивается лимфаденит в области трахеи и бронхов. Если у пациента сначала наблюдаются признаки сепсиса, но не наблюдаются бубоны, то такая форма называется первично септической. Однако это не значит, что лимфосистема не пострадала, просто на фоне интоксикации другие симптомы выражены слабо.
При септической чуме у человека довольно быстро развиваются вторичные очаги. Этот процесс стремительно подавляет иммунную систему, что в свою очередь приводит к быстрым дегенеративным изменениям во внутренних органах. Нарушается кровоснабжение в организме. Парез капилляров, внутрисосудистое свертывание крови, геморрагический синдром – это лишь одни из проявлений токсического шока. За ним следует почечная недостаточность и другие нарушения, которые приводят в смерти.
При воздушно-капельной передаче развивается первичная форма, опасная своей тяжестью и быстротой течения. Легочная ткань быстро атрофируется, некротизирует. Легочные альвеолы заполняются экссудатом, содержащим чумные палочки, лейкоциты, эритроциты.
Симптомы
Инкубационный период обычно длится до недели, а при легочной форме – сутки. Различные формы чумы дают разные симптомы. У восьмидесяти процентов больных диагностируют бубонную чуму, у пятнадцати – септическую и у пяти – легочную. Обычно болезнь начинается внезапно. У пациента повышается температура тела (около тридцати девяти и выше), начинается лихорадка, озноб. Явления интоксикации не заставляют себя ждать – это головная боль, разбитость, боль в мышцах, рвота, головокружение. Внешне может напоминать ОРЗ. Некоторые больные становятся беспокойными, мнительными, у них нарушается сознание, они бредят. По ночам возможны вскрикивания, попытки куда-то бежать. Речь становится непонятной, походка, словно у пьяного. Лицо пациента отекает, щеки свисают, кожа приобретает синий оттенок. Больные либо излишне напуганы, либо излишне флегматичны.
Кожа пациента сухая и горячая, лицо красное с синеватым оттенком и геморрагическими элементами. Слизистая оболочка рта красная с мелкими кровоизлияниями, миндалины отекают, на них образуется гнойный налет. Язык покрыт «температурным» (белым) налетом. Пульс учащен, но наполняемость сосудов слабая. Сердце прослушивается глухо. Отток мочи уменьшен, иногда возникает диарея, что в свою очередь приводит к обезвоживанию. Живот вздувается, селезенка и печень увеличены.
При кожной форме на покрове пациента возникает сначала пятно, а потом папула и пустула. Эти образования болезненны и наполнены кровянистым содержимым. После того, как пустула лопается, остаются изъязвления. Язвенное дно покрывается темным струпом, заживление происходит медленно с грубым рубцеванием.
При бубонной форме начальные симптомы характеризируются острейшим лимфаденитом. На месте образования бубона чувствуется местная гипертермия, гиперемия, болезненность, которая сковывает движения. Значительно количество бубонов возникает в паху – они могут увеличиваться до десяти сантиметров в диаметре. Помимо паха бубоны могут быть в подмышках, на шее. С вовлечением в патологический процесс окружающей клетчатки бубоны и принимают характерные черты. После этих больших бубонов могут возникать более мелкие отдаленные вторичные бубоны. С прогрессированием заболевания первичные бубоны становятся мягкими, при их пункции можно получить гнойное содержимое с примесью крови. При анализе содержимого обнаруживается большое количество чумных палочек. Если больного не лечить, то такие бубоны созревают сами, а потом вскрываются, оставляя свищи.
При первично-септической чуме явления интоксикации возникают внезапно и прогрессируют очень быстро – всего лишь за сутки. Человек ощущает лихорадку, озноб, головную боль, рвоту, тошноту, отсутствие аппетита, повышение температуры до сорока и выше. Лицо отекает, приобретает характерный красновато-синий оттенок. Артериальное давление понижено, пульс частый, но еле прощупывающийся. У пациентов развиваются проблемы с сердцем, начинаются геморрагии, в конце концов, приводящие к токсическому шоку. Если больным не оказать помощь, то они погибают за двое суток.
Вторично-септическая чума возникает, как правило, после бубонной. В этом случае состояние пациента крайне тяжелое, интоксикация происходит молниеносно. Наиболее часто – летальный исход.
Первично-легочная чума очень опасна в том плане, что передается самым простым путем. Так пациент может заразить достаточно большое количество людей. Болезнь протекает стремительно. Симптомы: лихорадка, озноб, высокая температура, нарушения психики, дыхания, координации движений. Если больные не получают лечения сразу же, то они умирают через шесть дней после того, как проконтактировали с источником.
Диагностика
Обычно диагностика основывается на первичных признаках и эпидемических данных. Особенно тщательно необходимо обследовать людей с подобными симптомами, прибывших из эпидемичных мест. Для того, чтобы не позволить распространиться болезни, люди с обнаруженными симптомами помещаются в специальные изоляторы. Чтобы поставить правильный диагноз, необходимо дифференцировать чуму с лимфаденитом, туляремией, лимфогранулематозом, сибирской язвой, пневмонией.
Более половины населения Европы в Средние века (XIV век) выкосила чума, известная как черная смерть. Ужас этих эпидемий остался в памяти людей по прошествии нескольких веков и даже запечатлен в полотнах художников. Далее чума неоднократно посещала Европу и уносила человеческие жизни, пусть и не в таких количествах.
В настоящее время заболевание чума остается . Около 2 тыс. человек заражается ежегодно. Из них большая часть умирает. Большинство случаев заражения отмечается в северных регионах Китая и странах Центральной Азии. По мнению специалистов для появления черной смерти сегодня нет причин и условий.
Возбудитель чумы был открыт в 1894 году. Изучая эпидемии заболевания, русские ученые разработали принципы развития заболевания, его диагностику и лечение, была создана противочумная вакцина.
Симптомы чумы зависят от формы заболевания. При поражении легких больные становятся высокозаразными, так как инфекция распространяется в окружающую среду воздушно-капельным путем. При бубонной форме чумы больные малозаразны или не заразны вовсе. В выделениях пораженных лимфоузлов возбудители отсутствуют, либо их совсем мало.
Лечение чумы стало значительно эффективнее с появлением современных антибактериальных препаратов. Смертность от чумы с этого времени снизилась до 70%.
Профилактика чумы включает в себя целый ряд мероприятий, ограничивающих распространение инфекции.
Чума является острым инфекционным зоонозным трансмиссивным заболеванием, которое в странах СНГ вместе с такими заболеваниями, как холера, туляремия и натуральная оспа считается (ООИ).
Рис. 1. Картина «Триумф смерти». Питер Брейгель.
Возбудитель чумы
В 1878 г. Г. Н. Минх и в 1894 г. А. Йерсен и Ш. Китазато, независимо друг от друга открыли возбудитель чумы. Впоследствии русские ученые изучили механизм развития заболевания, принципы диагностики и лечения, создали противочумную вакцину.
- Возбудитель заболевания (Yersinia pestis) представляет собой биполярную неподвижную коккобациллу, которая имеет нежную капсулу и никогда не образует спор. Способность образовывать капсулу и антифагоцитарную слизь не позволяет макрофагам и лейкоцитам активно бороться с возбудителем, в результате чего он быстро размножается в органах и тканях человека и животного, распространяясь с током крови и по лимфатическим путям по всему организму.
- Возбудители чумы выделяют экзотоксины и эндотоксины. Экзо- и эндотоксины содержаться в телах и капсулах бактерий.
- Ферменты агрессии бактерий (гиалуронидаза, коагулаза, фибринолизин, гемолизин) облегчают их проникновение в организм. Палочка способна проникать даже через неповрежденные кожные покровы.
- В грунте чумная палочка не теряет свою жизнеспособность до нескольких месяцев. В трупах животных и грызунов выживает до одного месяца.
- Бактерии устойчивы к низким температурам и замораживанию.
- Возбудители чумы чувствительны к высоким температурам, кислой реакции среды и солнечным лучам, которые убивают их только за 2 — 3 часа.
- До 30 дней возбудители сохраняются в гное, до 3 месяцев — в молоке, до 50 дней — в воде.
- Дезинфицирующие вещества уничтожают чумную палочку за несколько минут.
- Возбудители чумы вызывают заболевание у 250 видов животных. Среди них составляют большинство грызуны. Подвержены заболеванию верблюды, лисицы, кошки и другие животные.

Рис. 2. На фото чумная палочка — бактерия, вызывающая чуму — Yersinia pestis.
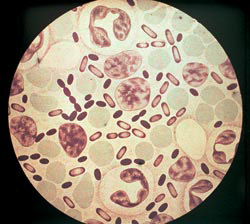
Рис. 3. На фото возбудители чумы. Интенсивность окраски анилиновыми красителями наибольшая на полюсах бактерий.
Php?post=4145&action=edit#
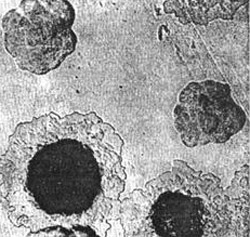
Рис. 4. На фото возбудители чумы — рост на плотной среде колонии. Вначале колонии похожи на битое стекло. Далее их центральная часть уплотняется, а периферия напоминает кружева.
Эпидемиология
Резервуар инфекции
Легко восприимчивы к чумной палочке грызуны (тарбаганы, сурки, песчанки, суслики, крысы и домовые мыши) и животные (верблюды, кошки, лисицы, зайцы, ежи и др). Из лабораторных животных подвержены инфекции белые мыши, морские свинки, кролики и обезьяны.
Собаки никогда не болеют чумой, но передают возбудитель через укусы кровососущих насекомых — блох. Погибшее от заболевания животное перестает быть источником инфекции. Если грызуны, инфицированные чумными палочками, впали в спячку, то заболевание у них приобретает латентное течение, а после спячки они вновь становятся распространителями возбудителей. Всего насчитывается до 250 видов животных, которые болеют, а значит являются источником и резервуаром инфекции.

Рис. 5. Грызуны — резервуар и источник возбудителя чумы.
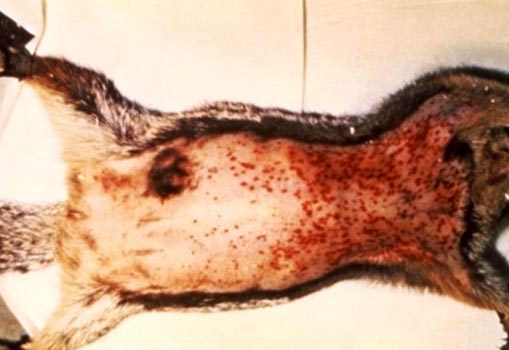
Рис. 6. На фото признаки чумы у грызунов: увеличенные лимфоузлы и множественные кровоизлияния под кожей.

Рис. 7. На фото малый тушканчик — переносчик заболевания чумой в Средней Азии.

Рис. 8. На фото черная крыса — переносчик не только чумы, но и лептоспироза, лейшманиоза, сальмонеллеза, трихинеллеза и др.
Пути заражения
- Основной путь передачи возбудителей — через укусы блох (трансмиссивный путь).
- Инфекция может попасть в организм человека при работе с больными животными: убой, снятие и разделка шкуры (контактный путь).
- Возбудители могут попасть в организм человека с зараженными продуктами питания, в результате их недостаточной термической обработки.
- От больного с легочной формой чумы инфекция распространяется воздушно-капельным путем.

Рис. 9. На фото блоха на коже человека.

Рис. 10. На фото момент укуса блохи.
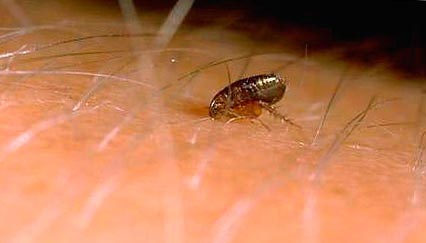
Рис. 11. Момент укуса блохи.
Переносчики возбудителя
- Переносчиками возбудителей являются блохи (в природе существует более 100 видов этих членистоногих насекомых),
- Переносчиками возбудителей являются некоторые виды клещей.
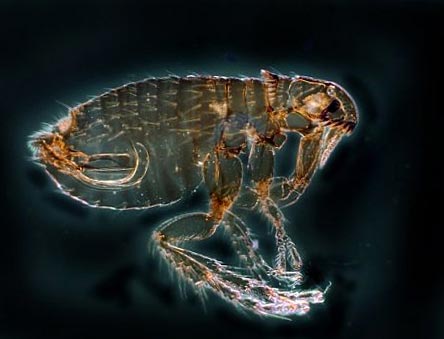
Рис. 12. На фото блоха – основной переносчик чумы. В природе существует более 100 видов этих насекомых.

Рис. 13. На фото сусликовая блоха – основной переносчик чумы.
Как происходит заражение
Заражение происходит через укус насекомого и втирание его фекалий и содержимого кишечника при срыгивании в процессе питания. При размножении бактерий в кишечной трубке блохи под воздействием коагулазы (фермента, выделяемого возбудителями) образуется «пробка», которая препятствует поступлению крови человека в ее организм. В результате чего блоха срыгивает сгусток на кожные покровы укушенного. Инфицированные блохи остаются высокозаразными в течение от 7 недель и до 1 года.

Рис. 14. На фото вид укуса блохи – пуликозное раздражение.
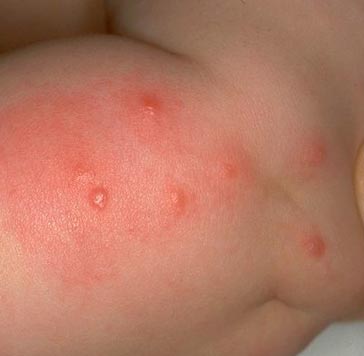
Рис. 15. На фото характерная серия укусов блохи.
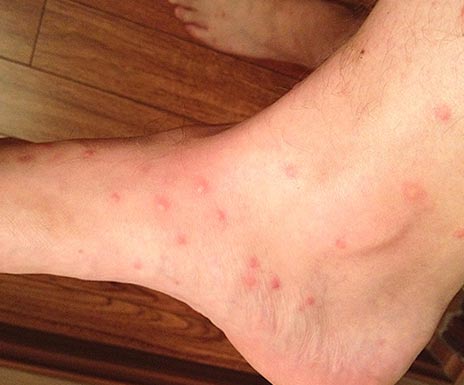
Рис. 16. Вид голени при укусах блох.
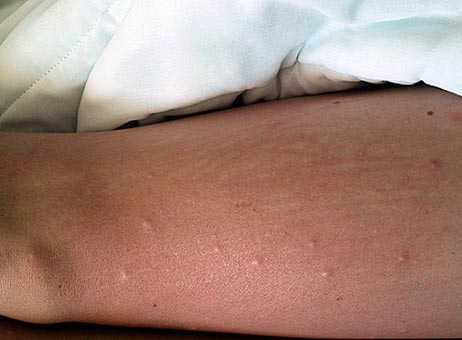
Рис. 17. Вид бедра при укусах блох.
Человек, как источник инфекции
- При поражении легких больные становятся высокозаразными. Инфекция распространяется в окружающую среду воздушно-капельным путем.
- При бубонной форме чумы больные малозаразны или не заразны вовсе. В выделениях пораженных лимфоузлов возбудители отсутствуют, либо их совсем мало.
Механизмы развития чумы
Способность чумной палочки образовывать капсулу и антифагоцитарную слизь не позволяет макрофагам и лейкоцитам активно с ней бороться, в результате чего возбудитель быстро размножается в органах и тканях человека и животного.
- Возбудители чумы через поврежденные кожные покровы и далее по лимфатическим путям проникают в лимфатические узлы, которые воспаляются и образуют конгломераты, (бубоны). На месте укуса насекомого развивается воспаление.
- Проникновение возбудителя в кровяное русло и его массивное размножение приводит к развитию бактериального сепсиса.
- От больного с легочной формой чумы инфекция распространяется воздушно-капельным путем. Бактерии попадают в альвеолы и вызывают тяжелую пневмонию.
- В ответ на массивное размножение бактерий организм больного вырабатывает огромное число медиаторов воспаления. Развивается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), при котором поражаются все внутренние органы. Особую опасность для организма представляют кровоизлияния в мышцу сердца и надпочечники. Развившийся инфекционно-токсический шок становится причиной гибели больного.
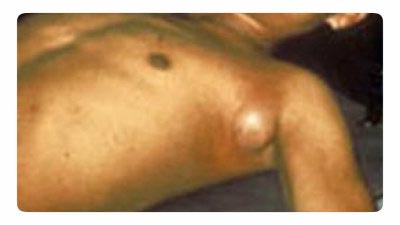
Рис. 18. На фото бубонная чума. Типичное увеличение лимфатического узла в подмышечной зоне.
Симптомы чумы
Болезнь проявляется после проникновения возбудителя в организм на 3 – 6 сутки (редко, но отмечены случаи проявления заболевания на 9 сутки). При попадании инфекции в кровь инкубационный период составляет несколько часов.
Клиническая картина начального периода
- Острое начало, большие цифры температуры и ознобы.
- Миалгии (мышечные боли).
- Мучительная жажда.
- Сильное проявление слабости.
- Быстрое развитие психомоторного возбуждения («очумелыми» называют таких больных). На лице появляется маска ужаса («маска чумы»). Реже отмечается заторможенность и апатия.
- Лицо становится гиперемированным и одутловатым.
- Язык густо обложен белым налетом («меловой язык»).
- На коже появляются множественные геморрагии.
- Значительно учащается сердечный ритм. Появляется аритмия. Падает артериальное давление.
- Дыхание становится поверхностным и учащенным (тахипноэ).
- Количество выделяемой мочи резко снижается. Развивается анурия (полное отсутствие выделения мочи).

Рис. 19. На фото помощь больному чумой оказывается медиками, одетыми в противочумные костюмы.
Формы заболевания чумой
Локальные формы заболевания
Кожная форма
На месте укуса блохи или контакта с инфицированным животным на кожных покровах появляется папула, которая быстро изъязвляется. Далее появляется черный струп и рубец. Чаще всего кожные проявления являются первыми признаками более грозных проявлений чумы.
Бубонная форма
Самая частая форма проявления заболевания. Увеличение лимфоузлов проявляется вблизи места укуса насекомого (паховые, подмышечные, шейные). Чаще воспаляется один лимфоузел, реже – несколько. При воспалении сразу нескольких лимфоузлов образуется болезненный бубон. Вначале лимфоузел твердой консистенции, болезненный при пальпации. Постепенно он размягчается, приобретая тестообразную консистенцию. Далее лимфоузел либо рассасывается, либо изъязвляется и склерозируется. Из пораженного лимфатического узла инфекция может попасть в кровяное русло, с последующим развитием бактериального сепсиса. Острая фаза бубонной формы чумы длится около недели.

Рис. 20. На фото пораженные шейные лимфоузлы (бубоны). Множественные кровоизлияния кожных покровов.
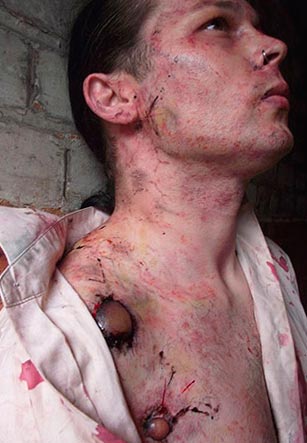
Рис. 21. На фото бубонная форма чумы — поражение шейных лимфоузлов. Множественные кровоизлияния в кожных покровах.

Рис. 22. На фото бубонная форма чумы.
Распространенные (генерализованные) формы
При попадании возбудителя в кровяное русло развиваются распространенные (генерализованные) формы чумы.
Первично-септическая форма
Если инфекция, минуя лимфоузлы, сразу попадает в кровь, то развивается первично-септическая форма заболевания. Молниеносно развивается интоксикация. При массивном размножении возбудителей в организме больного вырабатывается огромное число медиаторов воспаления. Это приводит к развитию синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдром), при котором поражаются все внутренние органы. Особую опасность для организма представляют кровоизлияния в мышцу сердца и надпочечники. Развившийся инфекционно-токсический шок становится причиной гибели больного.
Вторично-септическая форма заболевания
При распространении инфекции за пределы пораженных лимфоузлов и попадании возбудителей заболевания в кровяное русло развивается инфекционный сепсис, что проявляется резким ухудшением состояния больного, усилением симптомов интоксикации и развитием ДВС-синдрома. Развившийся инфекционно-токсический шок становится причиной гибели больного.

Рис. 23. На фото септическая форма чумы — последствия ДВС-синдрома.

Рис. 24. На фото септическая форма чумы — последствия ДВС-синдрома.
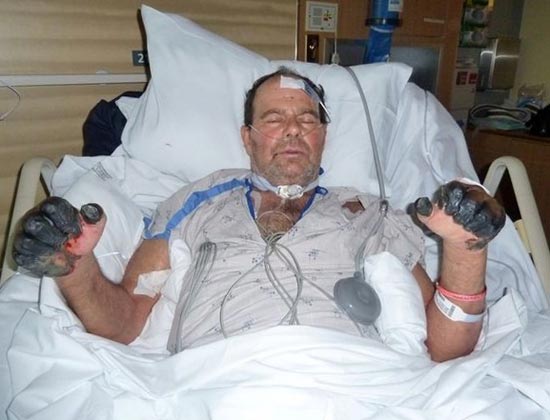
Рис. 25. 59-летний Пол Гэйлорд (житель города Портленд, штат Орегон, США). Бактерии чумы попали в его организм от бродячей кошки. В результате развившейся вторично-септической формы заболевания ему были ампутированы пальцы на руках и ногах.

Рис. 26. Последствия ДВС-синдрома.
Внешнедиссеминированные формы заболевания
Первично-легочная форма
Легочная форма чумы является самой тяжелой и опасной формой заболевания. Инфекция проникает в альвеолы воздушно-капельным путем. Поражение легочной ткани сопровождается кашлем и одышкой. Повышение температуры тела протекает с сильными ознобами. Мокрота вначале заболевания густая и прозрачная (стекловидная), потом становится жидкой и пенистой, с примесью крови. Скудные данные физикальных исследований не соответствуют тяжести заболевания. Развивается ДВС-синдром. Поражаются внутренние органы. Особую опасность для организма представляют кровоизлияния в сердечную мышцу и надпочечники. Смерть больного наступает от инфекционно-токсического шока.
При поражении легких больные становятся высокозаразными. Они формируют вокруг себя очаг особо опасного инфекционного заболевания.
Вторично-легочная форма
Является крайне опасной и тяжелой формой заболевания. Возбудители проникают в легочную ткань из пораженных лимфоузлов или с током крови при бактериальном сепсисе. Клиника и исход заболевания, как при первично-легочной форме.
Кишечная форма
Существование данной формы заболевания считается спорным. Предполагается, что заражение возникает с употреблением инфицированных продуктов. Вначале на фоне интоксикационного синдрома появляются боли в животе и рвота. Далее присоединяется понос и многочисленные позывы (тенезмы). Стул обильный слизисто-кровянистый.
Рис. 27. Фото противочумного костюма — особая экипировка медицинских работников при ликвидации очага особо опасного инфекционного заболевания.
Лабораторная диагностика чумы
Основой диагностики чумы является быстрое обнаружение чумной палочки. Вначале проводится бактериоскопия мазков. Далее выделяется культура возбудителя, которой заражаются подопытные животные.
Материалом для исследования служит содержимое бубона, мокрота, кровь, кал, кусочки ткани органов умерших и трупов животных.
Бактериоскопия
Возбудителем чумы (Yersinia pestis) является палочковидная биполярная коккобацилла. Анализ на обнаружение чумной палочки методом прямой бактериоскопии является наиболее простым и быстрым способом. Время ожидания результата составляет не более 2-х часов.
Посевы биологического материала
Культура возбудителя чумы выделяется в специализированных режимных лабораториях, предназначенных для работы с . Время роста культуры возбудителя составляет двое суток. Далее проводится тест на чувствительность к антибиотикам.
Серологические методы
Применение серологических методов позволяет определить наличие и рост антител в сыворотке крови больного к возбудителю чумы. Время получения результата составляет 7 дней.

Рис. 28. Диагностика чумы проводится в специальных режимных лабораториях.
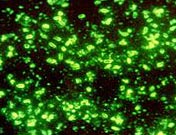
Рис. 29. На фото возбудители чумы. Флюоросцентная микроскопия.

Рис. 30. На фото культура Yersinia pestis.
Иммунитет при чуме
Антитела на внедрение возбудителя чумы образуются в достаточно поздние сроки развития заболевания. Иммунитет после перенесенного заболевания не длительный и не напряженный. Отмечаются повторные случаи заболевания, которые протекают так же тяжело, как и первые.
Лечение чумы
До начала лечения больной госпитализируется в отдельный бокс. Медицинский персонал, обслуживающий больного, одевается в специальный противочумный костюм.
Антибактериальное лечение
Антибактериальное лечение начинается при первых признаках и проявлениях заболевания. Из антибиотиков предпочтение отдается антибактериальным препаратам группы аминогликозидов (стрептомицин), группы тетрациклинов (вибромицин, морфоциклин), группы фторхинолонов (ципрофлоксацин), группы ансамицинов (рифампицин). Хорошо зарекомендовал себя при лечении кожной формы заболевания антибиотик группы амфениколов (кортримоксазол). При септических формах заболевания рекомендуется комбинация антибиотиков. Курс антибактериальной терапии составляет не менее 7 – 10 дней.
Лечение, направленное на разные этапы развития патологического процесса
Цель патогенетической терапии – снизить интоксикационный синдром путем выведения токсинов из крови больного.
- Показано введение свежезамороженной плазмы, белковых препаратов, реополиглюкина и других препаратов в сочетании с форсированным диурезом.
- Улучшение микроциркуляции достигается при применении трентала в сочетании с салкосерилом или пикамилоном.
- При развитии геморрагий немедленно проводится плазма-ферез с целью купирования синдрома диссеминированного внутрисосудистого свертывания.
- При падении давления назначается допамид. Это состояние говорит о генерализации и развитии сепсиса.
Симптоматическое лечение
Симптоматическое лечение нацелено на подавление и устранение проявлений (симптомов) чумы и, как следствие, облегчение страданий больного. Оно направлено на устранение боли, кашля, одышки, удушья, тахикардии и др.
Больной считается здоровым, если исчезли все симптомы заболевания и получено 3 отрицательных результата бактериологического исследования.
Противоэпидемические мероприятия
Выявление больного чумой является сигналом к незамедлительному проведению , которые включают в себя:
- проведение карантинных мероприятий;
- немедленная изоляция больного и проведение профилактического антибактериального лечения обслуживающего персонала;
- дезинфекция в очаге возникновения заболевания;
- вакцинация лиц, контактирующих с больным.
После прививки противочумной вакциной иммунитет сохраняется в течение года. Повторно прививаются через 6 мес. лица, которым угрожает повторное заражение: пастухи, охотники, работники сельского хозяйства и сотрудники противочумных учреждений.

Рис. 31. На фото бригада медиков одета в противочумные костюмы.
Прогноз заболевания
Прогноз заболевания чумой зависит от следующих факторов:
- формы заболевания,
- своевременности начатого лечения,
- наличия всего арсенала медикаментозного и немедикаментозного видов лечения.
Наиболее благоприятный прогноз у больных с поражением лимфоузлов. Смертность при этой форме заболевания достигает 5%. При септической форме заболевания показатель смертности достигает 95%.
Чума является и даже при применении всех необходимых лекарственных препаратов и манипуляций болезнь зачастую заканчивается смертью больного. Возбудители чумы постоянно циркулирует в природе и не поддается полному уничтожению и контролю. Симптомы чумы разнообразны и зависят от формы заболевания. Бубонная форма чумы является самой распространенной.
Статьи раздела "Особо опасные инфекции" Самое популярное
